Class 10 Science Chapter 4 question Answer In Assamese | SEBA Class 10 Science Question Answer
নমস্কাৰ, দশম শ্ৰেণীৰ বিজ্ঞান পাঠ্যপুথিৰ ৪ নং অধ্যায় “কাৰ্বন আৰু তাৰ যৌগ”ৰ সকলো পাঠভিত্তিক আৰু অনুশীলনীৰ প্ৰশ্নোত্তৰসমূহ, তলত সুন্দৰকৈ সজাই দিয়া হ’ল।
কাৰ্বন আৰু তাৰ যৌগ
পাঠভিত্তিক প্ৰশ্নোত্তৰ
পৃষ্ঠা নং – 61 (Page 61 in book)
প্ৰশ্ন ১: কাৰ্বন ডাই অক্সাইডৰ (CO₂) ৰ ইলেক্ট্ৰন বিন্দু গঠন কি হব?
উত্তৰ: কাৰ্বন ডাই অক্সাইডৰ (CO₂) ইলেক্ট্ৰন বিন্দু গঠন তলত দিয়া হ’ল:
কাৰ্বনৰ যোজ্যতা কক্ষত ৪টা ইলেক্ট্ৰন আৰু অক্সিজেনৰ যোজ্যতা কক্ষত ৬টা ইলেক্ট্ৰন থাকে। কাৰ্বনে দুটা অক্সিজেন পৰমাণুৰ লগত দ্বি-বান্ধনিৰে যুক্ত হৈ অষ্টক পূৰ্ণ কৰে।
O = C = O
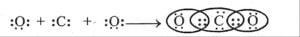
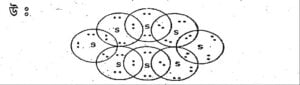
প্ৰশ্ন ২: আঠোটা ছালফাৰ পৰমাণুৰে গঠিত এটা ছালফাৰ অণুৰ ইলেক্ট্ৰন বিন্দু গঠন কি হব? (ইঙ্গিত—আঠটাকৈ ছালফাৰ পৰমাণু এটা বলয় আকৃতিত আছে।)
উত্তৰ: ছালফাৰৰ (S) যোজ্যতা কক্ষত ৬টা ইলেক্ট্ৰন থাকে। অষ্টক পূৰ্ণ কৰিবলৈ ইয়াক দুটা ইলেক্ট্ৰনৰ প্ৰয়োজন। S₈ অণুটোত, প্ৰতিটো ছালফাৰ পৰমাণুৱে ইয়াৰ কাষৰ দুটা ছালফাৰ পৰমাণুৰ লগত একোটা সহযোজী বান্ধনি গঠন কৰি এটা বলয় (ring) বা মুকুট (crown) আকৃতিৰ গঠন সৃষ্টি কৰে।
পৃষ্ঠা নং – 68 (Page 68 in book)
প্ৰশ্ন ১: পেন্টেনৰ বাবে কেইটা গঠন সমযোগী আঁকিব পাৰিবা?
উত্তৰ: পেন্টেনৰ (C₅H₁₂) বাবে তিনিটা গঠন সমযোগী (structural isomers) আঁকিব পাৰি:
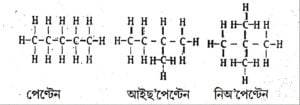
- n-পেন্টেন (n-pentane): এটা পোন শৃংখল।
CH₃–CH₂–CH₂–CH₂–CH₃ - আইছ’পেন্টেন (Isopentane) বা 2-মিথাইলবিউটেন: এটা শাখাযুক্ত শৃংখল।
CH₃–CH(CH₃)–CH₂–CH₃ - নিঅ’পেন্টেন (Neopentane) বা 2,2-ডাইমিথাইলপ্ৰ’পেন: এটা অধিক শাখাযুক্ত শৃংখল।
C(CH₃)₄
প্ৰশ্ন ২: কাৰ্বনৰ কোন দুটা ধৰ্মৰ বাবে আমি আমাৰ চাৰিওফালে অজস্ৰ কাৰ্বন-যৌগ পাওঁ?
উত্তৰ: কাৰ্বনৰ দুটা বিশেষ ধৰ্মৰ বাবে অজস্ৰ কাৰ্বন-যৌগ পোৱা যায়। সেই দুটা হ’ল:
কেটিনেচন (Catenation): কাৰ্বনে নিজৰ পৰমাণুৰ মাজতে সহযোজী বান্ধনি গঠন কৰি দীঘল শৃংখল, শাখাযুক্ত শৃংখল বা বলয় আকৃতিৰ যৌগ গঠন কৰিব পাৰে।
চতুৰ্সহযোজ্যতা (Tetravalency): কাৰ্বনৰ যোজ্যতা চাৰি। ইয়াৰ ফলত ই আন চাৰিটা কাৰ্বন পৰমাণু বা অন্য মৌলৰ (যেনে হাইড্ৰ’জেন, অক্সিজেন, নাইট্ৰ’জেন) পৰমাণুৰ লগত বান্ধনি গঠন কৰি বৃহৎ সংখ্যক যৌগ সৃষ্টি কৰিব পাৰে।
প্ৰশ্ন ৩: চাইক্ল’পেন্টেনৰ সংকেট আৰু ইলেক্ট্ৰনীয় বিন্দু গঠন লিখা।
উত্তৰ:
- আণৱিক সংকেট: C₅H₁₀
- গঠন: চাইক্ল’পেন্টেনত পাঁচটা কাৰ্বন পৰমাণুৱে এটা পঞ্চভুজীয় বলয় গঠন কৰে আৰু প্ৰতিটো কাৰ্বনৰ লগত দুটাকৈ হাইড্ৰ’জেন পৰমাণু সংযুক্ত হৈ থাকে।
- ইলেক্ট্ৰনীয় বিন্দু গঠন:
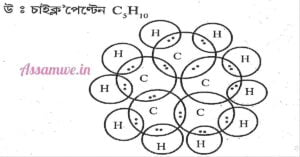
পৃষ্ঠা নং – 69 (Page 69 in book)
প্ৰশ্ন ৪: তলৰ যৌগবোৰৰ গঠন আঁকি দেখুওৱা-
(i) ইথানয়িক এছিড (ii) ব্ৰ’ম’পেন্টেন* (iii) বিউটান’ন (iv) হেক্সানেল
*ব্ৰ’ম’পেন্টেনৰ সমযোগী সম্ভৱনে?
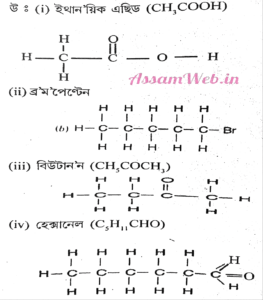
উত্তৰ:
(i) ইথানয়িক এছিড (Ethanoic acid): CH₃COOH
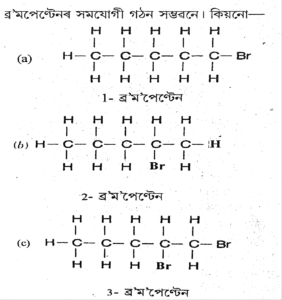
(ii) ব্ৰ’ম’পেন্টেন (Bromopentane): ইয়াৰ কেইবাটাও সমযোগী সম্ভৱ। যেনে:
* 1-ব্ৰ’ম’পেন্টেন: CH₃CH₂CH₂CH₂CH₂Br
* 2-ব্ৰ’ম’পেন্টেন: CH₃CH₂CH₂CH(Br)CH₃
(iii) বিউটান’ন (Butanone): CH₃COCH₂CH₃
(iv) হেক্সানেল (Hexanal): CH₃(CH₂)₄CHO
হয়, ব্ৰ’ম’পেন্টেনৰ গঠন সমযোগী সম্ভৱ। ব্ৰ’মিন (Br) পৰমাণুটো কাৰ্বন শৃংখলৰ বিভিন্ন স্থানত থাকিব পাৰে (যেনে 1-ব্ৰ’ম’পেন্টেন, 2-ব্ৰ’ম’পেন্টেন, 3-ব্ৰ’ম’পেন্টেন)।
প্ৰশ্ন ৫: তলৰ যৌগবোৰৰ নাম লিখা-
(i) CH₃–CH₂–Br
(ii) H–CHO
(iii) CH₃–C≡C–CH₂–CH₂–CH₃
উত্তৰ:
(i) ব্ৰ’ম’ইথেন (Bromoethane)
(ii) মিথানেল (Methanal)
(iii) হেক্স-২-আइन (Hex-2-yne)
পৃষ্ঠা নং – 71 (Page 71 in book)
প্ৰশ্ন ১: ইথানলক ইথানয়িক এচিডলৈ ৰূপান্তৰ কৰাটো কিয় এটা জাৰণ বিক্ৰিয়া?
উত্তৰ: ইথানলক (CH₃CH₂OH) ইথানয়িক এচিডলৈ (CH₃COOH) ৰূপান্তৰ কৰোঁতে ইথানলে অক্সিজেন গ্ৰহণ কৰে আৰু হাইড্ৰ’জেন হেৰুৱায়। যি বিক্ৰিয়াত অক্সিজেন যোগ হয় বা হাইড্ৰ’জেন আঁতৰ হয়, তাক জাৰণ বিক্ৰিয়া বোলা হয়। এই বিক্ৰিয়াটো ক্ষাৰকীয় KMnO₄ বা আম্লিক K₂Cr₂O₇ ৰ দৰে জাৰক দ্ৰব্যৰ উপস্থিতিত সংঘটিত হয়।
প্ৰশ্ন ২: লোহা জোৰা দিয়া সময়ত (welding) অক্সিজেন আৰু ইথাইন দহন কৰা হয়। ইথাইনৰ লগত বায়ু কিয় ব্যৱহাৰ কৰা নহয়?
উত্তৰ: লোহা জোৰা দিবলৈ অতি উচ্চ উষ্ণতাৰ প্ৰয়োজন। বিশুদ্ধ অক্সিজেনৰ লগত ইথাইন (C₂H₂) দহন কৰিলে এক অতি তাপবৰ্জী বিক্ৰিয়াৰ সৃষ্টি হয় (অক্সি-এচিটিলিন শিখা), যিয়ে প্ৰয়োজনীয় উচ্চ উষ্ণতা (প্ৰায় ৩০০০°C) প্ৰদান কৰে। ইয়াৰ বিপৰীতে, বায়ুত অক্সিজেনৰ উপৰিও নাইট্ৰ’জেনৰ দৰে নিষ্ক্ৰিয় গেছ থাকে। বায়ুৰ লগত ইথাইন দহন কৰিলে দহন অসম্পূৰ্ণ হয় আৰু উষ্ণতাও যথেষ্ট কম হয়, যি লোহা গলাবলৈ উপযুক্ত নহয়।
পৃষ্ঠা নং – ৮১ (Page 81 in book)
প্ৰশ্ন ১: পৰীক্ষাৰ সহায়ত এলক’হল আৰু কাৰ্বক্সিলিক এছিডৰ মাজৰ প্ৰভেদ কিদৰে দেখুৱাব পাৰি?
উত্তৰ: লিটমাছ পৰীক্ষাৰ দ্বাৰা। কাৰ্বক্সিলিক এছিডে (যেনে ইথানয়িক এছিড) নীলা লিটমাছ ৰঙা কৰিব, কাৰণ ই আম্লিক। কিন্তু এলক’হলে (যেনে ইথানল) লিটমাছৰ ৰং সলনি নকৰে, কাৰণ ই প্ৰশম।
প্ৰশ্ন ২: জাৰক দ্ৰব্য কি?
উত্তৰ: যিবোৰ পদাৰ্থই আন পদাৰ্থক জাৰিত কৰিবলৈ অক্সিজেন যোগান ধৰিব পাৰে, সেইবোৰক জাৰক দ্ৰব্য (Oxidising agent) বোলে। উদাহৰণ: ক্ষাৰকীয় পটাছিয়াম পাৰমেঙ্গানেট (KMnO₄) বা আম্লিক পটাছিয়াম ডাইক্ৰ’মেট (K₂Cr₂O₇)।
অনুশীলনী
পৃষ্ঠা নং – ৮৪-৮৫ (Page 84-85 in PDF)
প্ৰশ্ন ১: ইথেন (C₂H₆) অণু এটাত –
উত্তৰ: (b) 7 টা সহযোজী বান্ধনি আছে। (6 টা C-H আৰু 1 টা C-C বান্ধনি)
প্ৰশ্ন ২: চাৰিটা কাৰ্বনৰ যৌগ বিউটান’নত থকা কাৰ্য কৰী মূলক হ’ল—
উত্তৰ: (c) কিট’ন
প্ৰশ্ন ৩: ৰন্ধনৰ সময়ত ব্যৱহৃত বৰ্তনৰ তলফালে (বাহিৰত) ক’লা পৰে কিয়নো—
উত্তৰ: (b) ইন্ধনটো সম্পূৰ্ণৰূপে দহন নহয়।
প্ৰশ্ন ৪: CH₃Cl ৰ উদাহৰণ লৈ সহযোজী বান্ধনিৰ স্বৰূপ (nature) ব্যাখ্যা কৰা।
উত্তৰ: CH₃Cl (ক্ল’ৰ’মিথেন)ত কাৰ্বনে তিনিটা হাইড্ৰ’জেন পৰমাণু আৰু এটা ক্ল’ৰিন পৰমাণুৰ লগত ইলেক্ট্ৰনৰ ভাগ-বতৰা কৰি চাৰিটা একক সহযোজী বান্ধনি গঠন কৰে। ইয়াত কোনো আয়নৰ সৃষ্টি নহয়। এনে বান্ধনিবোৰ সাধাৰণতে দুৰ্বল আন্তঃআণৱিক বলৰ দ্বাৰা গঠিত আৰু ইহঁতৰ গলনাংক আৰু উতলাংক কম হয়। ইহঁত বিদ্যুৎৰ কুপৰিবাহী।
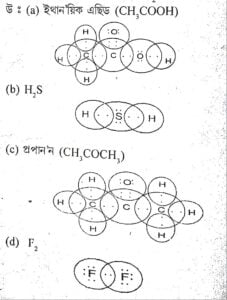
প্ৰশ্ন ৫: তলত দিয়াবিলাকৰ ইলেক্ট্ৰন বিন্দু গঠন লিখা—
(a) ইথানয়িক এছিড (b) H₂S (c) প্ৰপান’ন (d) F₂
উত্তৰ:
প্ৰশ্ন ৬: সমগণীয় শ্ৰেণী কাক বোলে? উদাহৰণ দি বুজাই লিখা।
উত্তৰ: একে কাৰ্যকৰী মূলকযুক্ত কাৰ্বন যৌগৰ এনে এটা শ্ৰেণীক সমগণীয় শ্ৰেণী বোলা হয়, য’ত শৃংখলত থকা হাইড্ৰ’জেন পৰমাণুক একে কাৰ্যকৰী মূলকে প্ৰতিষ্ঠাপন কৰে। এই শ্ৰেণীৰ সদস্যবোৰৰ মাজত –CH₂ গোটৰ পাৰ্থক্য থাকে। উদাহৰণ: এলক’হলৰ সমগণীয় শ্ৰেণী – মিথানল (CH₃OH), ইথানল (C₂H₅OH), প্ৰ’পানল (C₃H₇OH), ইত্যাদি।
প্ৰশ্ন ৭: ভৌতিক আৰু ৰাসায়নিক ধৰ্মৰ ওপৰত ভিত্তি কৰি ইথানল আৰু ইথানয়িক এচিডৰ পাৰ্থক্য লিখা।
উত্তৰ:
| বৈশিষ্ট্য | ইথানল (Ethanol) | ইথানয়িক এছিড (Ethanoic Acid) |
|---|---|---|
| গোন্ধ | মিঠা, এলক’হলীয় গোন্ধ। | টেঙা, ভিনেগাৰৰ দৰে গোন্ধ। |
| লিটমাছ পৰীক্ষা | লিটমাছৰ ৰং সলনি নকৰে (প্ৰশম)। | নীলা লিটমাছ ৰঙা কৰে (আম্লিক)। |
| Na₂CO₃ ৰ লগত বিক্ৰিয়া | কোনো বিক্ৰিয়া নঘটে। | CO₂ গেছৰ বুৰবুৰণি উঠে। |
| গলনাংক | ১৫৬ K | ২৯০ K |
প্ৰশ্ন ৮: পানীত চাবোন দিলে কিয় ফেন উঠে? বেলেগ দ্ৰাৱক যেনে ইথানলত ফেন উঠিবনে?
উত্তৰ: চাবোনৰ অণুৰ দুটা মূৰ থাকে – এটা জলস্নেহী (hydrophilic) আৰু আনটো জলবিদ্বেষী (hydrophobic)। পানীত দিলে, জলবিদ্বেষী মূৰবোৰ একত্ৰিত হৈ মাইছেল (micelle) গঠন কৰে, যাৰ ফলত ফেন উঠে। ইথানলৰ দৰে দ্ৰাৱকত চাবোনে মাইছেল গঠন নকৰে, কাৰণ ইথানলত জলবিদ্বেষী অংশ দ্ৰৱীভূত হয়। সেয়েহে ফেন নুঠে।
প্ৰশ্ন ৯: প্ৰায় সকলো ক্ষেত্ৰতে কাৰ্বন আৰু ইয়াৰ যৌগ ইন্ধন হিচাপে ব্যৱহাৰ হয়। কিয়?
উত্তৰ: কাৰ্বন আৰু ইয়াৰ যৌগবোৰ দহন কৰিলে প্ৰচুৰ পৰিমাণে তাপ আৰু পোহৰ শক্তি উৎপন্ন হয়। ইহঁতৰ কেলৰিফিক মান (calorific value) উচ্চ আৰু দহন নিয়ন্ত্ৰণ কৰিব পাৰি। সেয়েহে ইহঁতক ইন্ধন হিচাপে ব্যৱহাৰ কৰা হয়।
প্ৰশ্ন ১০: কঠিন পানীত চাবোন ব্যৱহাৰ কৰিলে গেদ (scum) কিদৰে সৃষ্টি হয় ব্যাখ্যা কৰা।
উত্তৰ: কঠিন পানীত কেলছিয়াম (Ca²⁺) আৰু মেগনেছিয়াম (Mg²⁺) আয়ন থাকে। চাবোনে এই আয়নবোৰৰ লগত বিক্ৰিয়া কৰি অদ্ৰৱণীয় পদাৰ্থৰ অধঃক্ষেপ সৃষ্টি কৰে, যাক গেদ (scum) বোলা হয়। ই চাফাই কাৰ্যত বাধা দিয়ে।
প্ৰশ্ন ১১: নীলা আৰু ৰঙা লিটমাছ কাগজেৰে চাবোন পৰীক্ষা কৰিলে কি দেখিবা?
উত্তৰ: চাবোন ক্ষাৰকীয় প্ৰকৃতিৰ। সেয়েহে ই ৰঙা লিটমাছ নীলা কৰিব, কিন্তু নীলা লিটমাছৰ কোনো ৰং সলনি নকৰে।
প্ৰশ্ন ১২: হাইড্ৰ’জেনেচন মানে কি? ইয়াৰ ঔদ্যোগিক প্ৰয়োগ লিখা।
উত্তৰ: নিকেল বা পেলাডিয়াম অনুঘটকৰ উপস্থিতিত অসংপৃক্ত হাইড্ৰ’কাৰ্বনৰ লগত হাইড্ৰ’জেন যোগ হৈ সংপৃক্ত হাইড্ৰ’কাৰ্বনলৈ ৰূপান্তৰিত হোৱা বিক্ৰিয়াকে হাইড্ৰ’জেনেচন বোলা হয়।
ঔদ্যোগিক প্ৰয়োগ: এই পদ্ধতিৰে উদ্ভিদজাত তেলৰ পৰা বনস্পতি ঘি (ডালডা) প্ৰস্তুত কৰা হয়।
প্ৰশ্ন ১৩: তলৰ কোনবিলাকৰ হাইড্ৰ’কাৰ্বনে যোগাত্মক বিক্ৰিয়া দেখুৱায়?
C₂H₆, C₃H₈, C₃H₆, C₂H₂, আৰু CH₄
উত্তৰ: C₃H₆ (প্ৰ’পিন) আৰু C₂H₂ (ইথাইন)। কাৰণ ইহঁত অসংপৃক্ত হাইড্ৰ’কাৰ্বন (দ্বিবান্ধনি আৰু ত্ৰিবান্ধনি যুক্ত)।
প্ৰশ্ন ১৪: মাখন (butter) আৰু খোৱাতেলৰ (cooking oil) মাজত পাৰ্থক্য দেখুৱাব পৰা এটা পৰীক্ষা বৰ্ণনা কৰা।
উত্তৰ: মাখন হ’ল সংপৃক্ত যৌগ আৰু খোৱাতেল হ’ল অসংপৃক্ত যৌগ। ক্ষাৰকীয় KMnO₄ দ্ৰৱৰ লগত পৰীক্ষা কৰিলে, খোৱাতেলে দ্ৰৱটোৰ বেঙুনীয়া ৰং নাইকিয়া কৰিব (যোগাত্মক বিক্ৰিয়া), কিন্তু মাখনে নকৰে।
প্ৰশ্ন ১৫: চাবোনৰ মলি আঁতৰোৱাৰ প্ৰক্ৰিয়া (cleaning action) ব্যাখ্যা কৰা।
উত্তৰ: চাবোনৰ অণুবোৰে পানীত মাইছেল গঠন কৰে। মাইছেলৰ জলবিদ্বেষী অংশই তেলীয়া মলিৰ লগত বান্ধনি গঠন কৰে আৰু জলস্নেহী অংশ বাহিৰফালে পানীত থাকে। পানীৰে ধুলে এই মাইছেলবোৰ মলিৰ সৈতে আঁতৰি যায়, যাৰ ফলত কাপোৰ চাফা হয়।
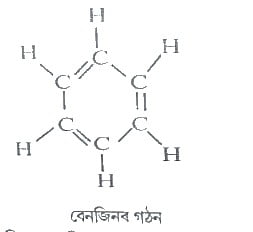
প্রঃ ৪৩। বেনজিনৰ সংকেত কি? ইয়াৰ গঠন দেখুওৱা।
বেনজিনৰ সংকেত – C6H6